Encefalite por Varicela Zoster em Viajante Imunocompetente
Conteúdo do artigo principal
Resumo
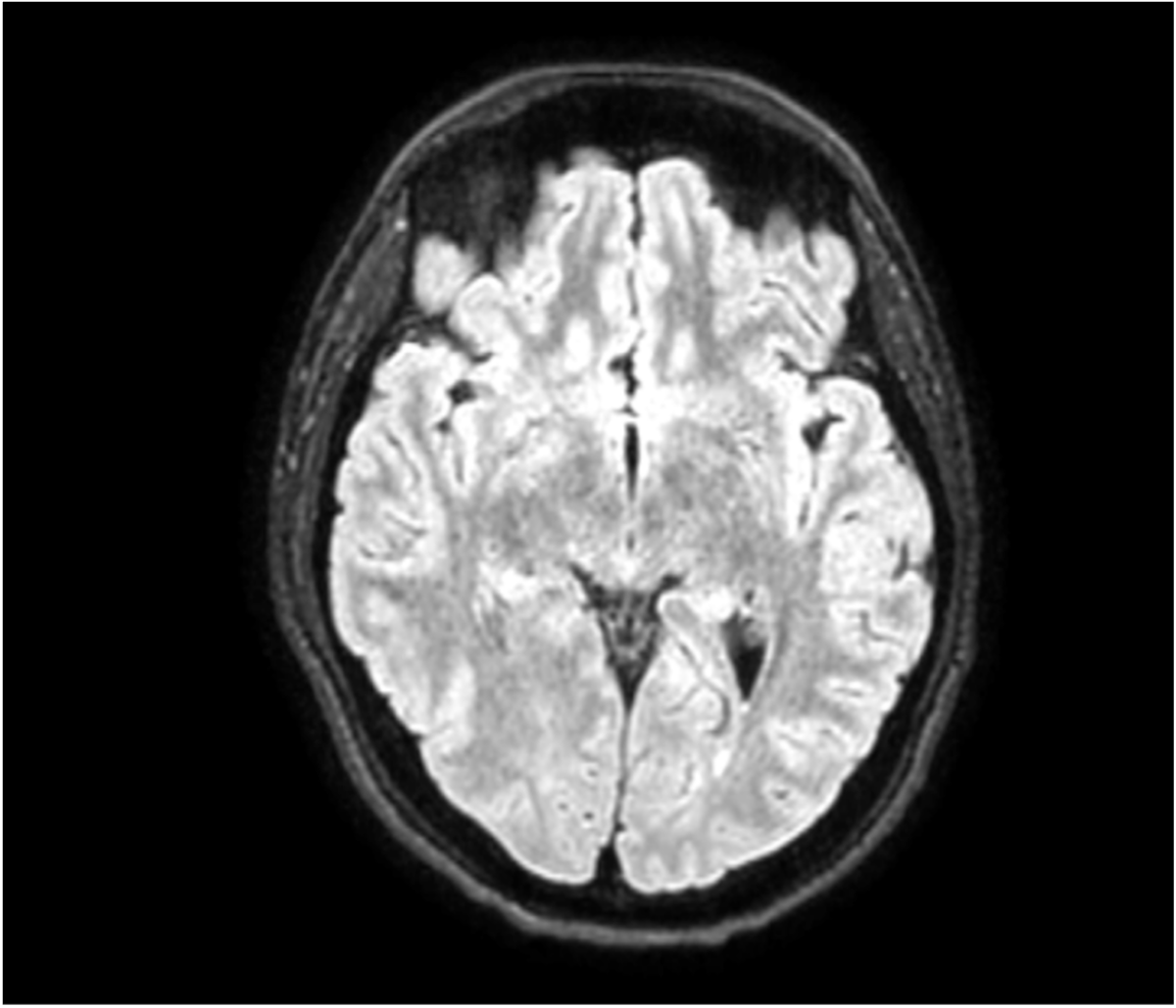
O vírus varicela-zoster (VZV) é causa frequente de encefalite em adultos, especialmente idosos e imunodeprimidos. Em jovens imunocompetentes e sem manifestações cutâneas, trata-se de apresentação rara. Relata-se o caso de um homem de 35 anos, previamente hígido, que desenvolveu encefalite por VZV durante viagem de dez meses pela América Latina. Na Nicarágua, apresentou cefaleia bitemporal e suboccipital esquerda, pulsátil, insidiosa, diária, com piora progressiva. Após cinco dias, procurou atendimento por distúrbio de linguagem (parafasias). Negava febre, convulsões, paresias ou sintomas sistêmicos. Ao exame físico, apresentava apenas alterações de linguagem, sem lesões cutâneas. Ressonância magnética mostrou hiperintensidade em lobo temporal esquerdo. O líquor apresentou hipoglicorraquia, hiperproteinorraquia e hiperlactatorraquia. Teste molecular (PCR) detectou DNA do VZV. Iniciou-se aciclovir intravenoso por oito dias, seguido de aciclovir oral por seis, com resolução completa do quadro, sem déficits residuais. Investigação de imunodeficiência, incluindo testes para HIV, imunofenotipagem linfocitária, imunoglobulinas e complemento, foi negativa. Como profilaxia, foi recomendada vacinação com vacina recombinante inativada contra herpes zoster. O caso ilustra uma forma atípica de encefalite por VZV, reforçando a importância dos testes moleculares na investigação de quadros neurológicos agudos e do tratamento antiviral precoce para bom prognóstico.
Detalhes do artigo

Este trabalho está licenciado sob uma licença Creative Commons Attribution 4.0 International License.
Authors retain the copyright of their articles and grant the journal the right of first publication under the Creative Commons Attribution (CC BY) license, which allows others to share and adapt the work with proper attribution.
Referências
Kennedy PGE. Varicella-zoster virus latency in human ganglia. Rev Med Virol. 2002;12(5):327–34. doi:10.1016/0022-3956(75)90026-6
Kennedy PGE, Gershon AA. Clinical features of varicella-zoster virus infection. Viruses. 2018;10(11):609. doi:10.3390/v10110609
George BP, Schneider EB, Venkatesan A. Encephalitis hospitalization rates and inpatient mortality in the United States, 2000–2010. PLoS One. 2014;9(9):e104169. doi:10.1371/journal.pone.0104169
Alvarez JC, Alvarez J, Ticono J, Medallo P, Miranda H, Ferrés M, et al. Varicella-zoster virus meningitis and encephalitis: an understated cause of central nervous system infections. Cureus. 2020;12(11):e11603. doi:10.7759/cureus.11583
Bodilsen J, Storgaard M, Larsen L, Wiese L, Helweg-Larsen J, Lebech AM, et al. Infectious meningitis and encephalitis in adults in Denmark: a prospective nationwide observational cohort study (DASGIB). Clin Microbiol Infect. 2018;24(10):1102.e1–5. doi:10.1016/j.cmi.2018.01.016
Picard L, Mailles A, Fillâtre P, Tattevin P, Stahl JP. Encephalitis in travellers: a prospective multicentre study. J Travel Med. 2023;30(2):taad013. doi:10.1093/jtm/taac145
Herlin LK, Hansen KS, Bodilsen J, Larsen L, Brandt C, Andersen CØ, et al. Varicella zoster virus encephalitis in Denmark from 2015 to 2019: a nationwide prospective cohort study. Clin Infect Dis. 2021;72(7):1192–9. doi:10.1093/cid/ciaa185
Chamizo FJ, Gilarranz R, Hernández M, Ramos D, Pena MJ. Central nervous system infections caused by varicella-zoster virus. J Neurovirol. 2016;22(4):529–32. doi:10.1007/s13365-016-0422-y
Lenfant T, L’Honneur AS, Ranque B, Pilmis B, Charlier C, Zuber M, et al. Neurological complications of varicella zoster virus reactivation: prognosis, diagnosis, and treatment of 72 patients with positive PCR in the cerebrospinal fluid. Brain Be-hav. 2022;12(2):e2496. doi:10.1002/brb3.2455
Pahud BA, Glaser CA, Dekker CL, Arvin AM, Schmid DS. Varicella zoster disease of the central nervous system: epidemio-logical, clinical, and laboratory features 10 years after the introduction of the varicella vaccine. J Infect Dis. 2011;203(3):316–23. doi:10.1093/infdis/jiq066
Kaewpoowat Q, Salazar L, Aguilera E, Wootton SH, Hasbun R. Herpes simplex and varicella zoster CNS infections: clinical presentations, treatments and outcomes. Infection. 2016;44(3):337–45. doi:10.1007/s15010-015-0867-6
Skripuletz T, Pars K, Schulte A, Schwenkenbecher P, Yildiz Ö, Ganzenmueller T, et al. Varicella zoster virus infections in neurological patients: a clinical study. BMC Infect Dis. 2018;18(1):238. doi:10.1186/s12879-018-3137-2
Folstein MF, Folstein SE, McHugh PR. “Mini-mental state”: a practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res. 1975;12(3):189–98. doi:10.1016/0022-3956(75)90026-6
Nasreddine ZS, Phillips NA, Bédirian V, Charbonneau S, Whitehead V, Collin I, et al. The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J Am Geriatr Soc. 2005;53(4):695–9. doi:10.1111/j.1532-5415.2005.53221.x
Goswami S, Goyal R, DeLury J. A possible case of varicella zoster virus (VZV) meningoencephalitis in an immunocompetent host. Cureus. 2022;14(7):e26597. doi:10.7759/cureus.26539
Robertson KM, Harvey CL, Cunningham JM. Acyclovir-induced neurotoxicity with a positive cerebrospinal fluid varicella zoster PCR result creating a management dilemma: a case report. J Med Case Rep. 2020;14(1):171. doi:10.1186/s13256-020-02498-3
Salvotti F, Trapletti S, Chiarini G, Castellano M, Muiesan ML. Atypical varicella-zoster virus reactivation: a case report. Eur J Case Rep Intern Med. 2023;10(9):003866. doi:10.12890/2023_003945
Ministério da Saúde (BR). Portaria SECTICS/MS nº 61, de 16 de dezembro de 2024. Torna pública a decisão de incorporar, no âmbito do Sistema Único de Saúde – SUS, o teste de PCR multiplex para agentes infecciosos de meningite e encefalite. Di-ário Oficial da União. Brasília (DF); 2024 dez 18 [citado 2025 out 7]. Disponível em: https://bvs.saude.gov.br/bvs/saudelegis/sctie/2024/prt0061_18_12_2024.html
Comissão Nacional de Incorporação de Tecnologias no SUS (CONITEC). Relatório de Recomendação nº 938: Teste PCR multiplex para diagnóstico de meningite e encefalite. Brasília (DF): Ministério da Saúde; 2024 [citado 2025 out 7]. Disponí-vel em: https://www.gov.br/conitec/pt-br/midias/relatorios/2024/relatorio-de-recomendacao-no-938_pcr-multiplex-meningite_encefalite.pdf
Agência Nacional de Saúde Suplementar (ANS). Resolução Normativa nº 627, de 14 de fevereiro de 2025. Atualiza o Rol de Procedimentos e Eventos em Saúde, incluindo o exame “Agentes infecciosos na encefalite e meningite – detecção por PCR multiplex em painel no líquor”. Diário Oficial da União. Brasília (DF); 2025 fev 17 [citado 2025 out 7]. Disponível em: https://www.gov.br/ans/pt-br/assuntos/gestao-da-saude/rol-de-procedimentos/.